
Một buổi trị liệu bằng âm nhạc của các bệnh nhân Alzheimer tại Trung tâm chăm sóc Copper Ridge ở thị trấn Sykesville, bang Maryland, Mỹ - Ảnh: AFP
Tôi nghĩ họ đã quyết định đúng. Việc phê duyệt sẽ giúp thuốc sẵn sàng [để điều trị] cho người bệnh trong khi vẫn yêu cầu công ty phải nghiên cứu thêm để chứng minh lợi ích của thuốc.
Bác sĩ Howard Fillit (làm việc tại Quỹ khám phá thuốc Alzheimer - ADDF)
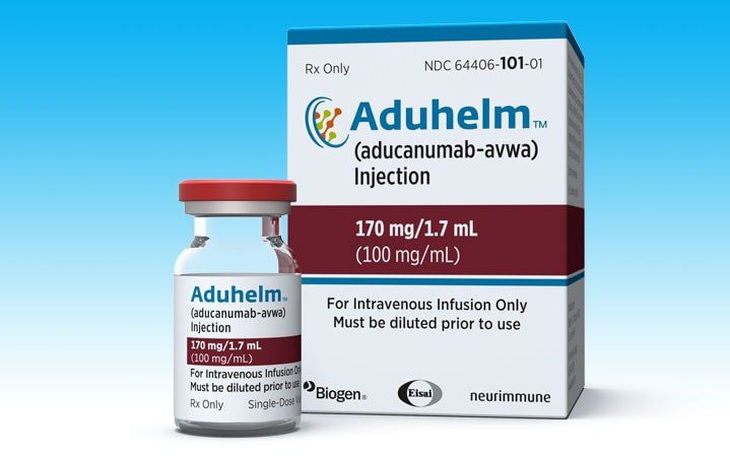
Thuốc aducanumab (tên biệt dược là Aduhelm) là loại thuốc đầu tiên nhắm vào nguyên nhân cơ bản gây bệnh Alzheimer chứ không chỉ điều trị các triệu chứng như các thuốc khác.
Vì sao phê duyệt nhanh?
Mặc dù đây là thông tin rất đáng chú ý, song cần phải nhấn mạnh rằng thuốc aducanumab mới được FDA phê chuẩn nhanh (accelerated approval) chứ chưa phải đã được phê duyệt chính thức (full approval).
FDA Mỹ áp dụng chương trình phê duyệt nhanh với các loại thuốc điều trị bệnh nghiêm trọng hoặc đe dọa tính mạng và chưa có lựa chọn thay thế.
Lộ trình này được sử dụng khi FDA tin rằng một loại thuốc có thể mang lại lợi ích lớn hơn các phương pháp điều trị hiện có dù vẫn còn một số điều không chắc chắn.
Sau khi được phê duyệt nhanh, các công ty dược sẽ tiếp tục thực hiện thêm các nghiên cứu để xác nhận lợi ích lâm sàng trong giai đoạn thương mại hóa (tức thử nghiệm giai đoạn 4), việc này có thể mất vài năm.
Nếu kết quả nghiên cứu phản ánh đúng lợi ích lâm sàng, FDA sẽ phê duyệt chính thức. Còn không, thuốc có thể bị rút khỏi thị trường.
Thuốc Aduhelm do Công ty Biogen của Mỹ hợp tác với Công ty Eisai của Nhật Bản phát triển. Thuốc tiêm qua đường tĩnh mạch hằng tháng nhằm làm chậm lại tình trạng suy giảm nhận thức và trí nhớ ở người bệnh Alzheimer. Thuốc đã trải qua hai thử nghiệm lâm sàng giai đoạn cuối (giai đoạn 3).
Aduhelm chỉ làm giảm tình trạng suy giảm nhận thức ở một trong hai thử nghiệm trên. Tuy nhiên, trong cả hai thử nghiệm, thuốc cho thấy có sự giảm rõ rệt những tích tụ của một loại protein gọi là amyloid beta trong mô não của bệnh nhân Alzheimer.
Nguyên nhân gây ra Alzheimer chưa được hiểu rõ. Một giả thiết cho rằng Alzheimer là do sự tích tụ quá nhiều amyloid beta trong não một số người khi già đi và hệ miễn dịch bị suy giảm. Do đó, cung cấp aducanumab cho bệnh nhân Alzheimer có thể giúp họ giảm bớt các mảng tích tụ này.
Theo báo New York Times, FDA thừa nhận các thử nghiệm lâm sàng của thuốc Aduhelm chưa cung cấp đủ bằng chứng cho thấy hiệu quả. Song bà Patrizia Cavazzoni - giám đốc Trung tâm Nghiên cứu và đánh giá dược phẩm của FDA - khẳng định "quyết định phê duyệt là phù hợp".
Bà Alisha Alaimo, chủ tịch Công ty Biogen, cho biết công ty cam kết hỗ trợ những bệnh nhân thu nhập thấp có thể điều trị bằng Aduhelm. Chi phí điều trị hằng năm bằng thuốc Aduhelm là 56.000 USD nhưng tùy loại bảo hiểm, người bệnh có thể sẽ được giảm bớt chi phí đó.
Còn nhiều tranh cãi
Công ty Biogen và một số nhà thần kinh học ca ngợi quyết định của FDA, nhưng một số nhà khoa học khác muốn chờ thêm bằng chứng.
"Thay mặt những người bị Alzheimer và tất cả các bệnh làm sa sút trí tuệ khác, chúng tôi ca ngợi quyết định lịch sử ngày hôm nay" - Hiệp hội Alzheimer, một tổ chức phi lợi nhuận của Mỹ, viết trên Twitter ngày 7-6.
Tuy nhiên, bác sĩ Ronald Petersen, chuyên gia bệnh Alzheimer tại Trung tâm y tế Mayo Clinic (Mỹ), cảnh báo đây không phải là thuốc trị dứt điểm căn bệnh, mà chỉ "hy vọng làm chậm tiến triển bệnh".
Theo Hãng tin Reuters, một số nhà khoa học hy vọng việc FDA cấp phép cho Aduhelm sẽ là yếu tố giúp thúc đẩy các loại thuốc tốt hơn được phát triển.
Các nhà phân tích Phố Wall dự đoán việc FDA phê chuẩn thuốc của Biogen sẽ giúp phục hồi một lĩnh vực đã bị nhiều công ty dược phẩm lớn từ bỏ sau những chuỗi dài thất bại.
Trước Aduhelm, loại thuốc trị Alzheimer gần nhất được phê chuẩn vào năm 2003. Tất cả các loại thuốc trị Alzheimer trước Aduhelm mới chỉ cố gắng giảm bớt các triệu chứng chứ chưa giải quyết được nguyên nhân gốc rễ căn bệnh.
Trong khi đó, bác sĩ Caleb Alexander, nhà nghiên cứu dược phẩm tại ĐH Johns Hopkins và là thành viên hội đồng chuyên gia độc lập của FDA, nói: "Tôi ngạc nhiên và thất vọng". Theo bác sĩ Alexander, khó có nhà khoa học nào cảm thấy thuyết phục trước các bằng chứng thử nghiệm lâm sàng của thuốc Aduhelm.
Trước đó, vào tháng 11-2020, hội đồng chuyên gia độc lập của FDA cho rằng họ không thấy đủ bằng chứng về lợi ích của Aduhelm và đã đề nghị FDA không phê duyệt thuốc này.
50 triệu
Bệnh Alzheimer ảnh hưởng đến khoảng 50 triệu người trên thế giới và thường xuất hiện ở những người từ 65 tuổi trở lên. Bệnh phá hủy từ từ các mô não, làm họ mất dần trí nhớ, khả năng ngôn ngữ và năng lực tư duy. Cuối cùng, bệnh nhân không thể hoàn thành ngay cả những việc đơn giản nhất.
Bệnh thường tiến triển chậm, bắt đầu với biểu hiện đãng trí nhẹ thoáng qua. Khi đến giai đoạn cuối, bệnh nhân thường bị tổn thương não nghiêm trọng. Alzheimer là nguyên nhân gây tử vong cao thứ 6 ở Mỹ.











Tối đa: 1500 ký tự
Hiện chưa có bình luận nào, hãy là người đầu tiên bình luận